Allergie – was ist das?
Allergien werden immer häufiger. Das gilt für Kinder, aber auch für Erwachsene. Sie können selbst im hohen Alter noch Allergien entwickeln. Wann spricht man eigentlich von einer Allergie? Kennt man die Ursachen? Wie zeigen sich die Symptome? Wie wird die Diagnose gestellt und welche Therapien stehen aktuell zur Verfügung? Erfahren Sie mehr in diesem MeinAllergiePortal-Überblick. Alles über Ursachen, Symptome, Diagnose und Therapie.
Autor: Dr. Susanne Meinrenken, Prof. Dr. med. Torsten Zuberbier, Angela Balatoni, Prof. Dr. med. Thilo Jakob
Was ist eigentlich eine Allergie?
Eine Allergie ist eigentlich eine Überreaktion des Immunsystems: Das Immunsystem reagiert mit einer spezifischen Überempfindlichkeit auf bestimmte körperfremde Stoffe. Solche Substanzen, die zu einer Allergie führen, nennt man Allergene. Damit es zu einer allergischen Reaktion kommen kann, muss das Immunsystem mindestens zweimal mit dem Allergen in Kontakt gekommen sein. Nach dem Erstkontakt kann es zu einer Sensibilisierung kommen, das heißt, einer Allergiebereitschaft. Dies ist die Voraussetzung für eine mögliche allergische Reaktion bei dem nächsten Kontakt. Allerdings können Menschen auch eine Sensibilisierung gegenüber bestimmten Substanzen aufweisen, ohne allergisch darauf zu reagieren.
Welche allergischen Erkrankungen gibt es?
Eine ganze Reihe von Erkrankungen wird zu den allergischen Erkrankungen gezählt: die allergische Rhinitis beziehungsweise Rhinokonjunktivitis, also eine allergische Reaktion, die die Nase beziehungsweise Nase und Augen betrifft, auch Heuschnupfen genannt, allergisches Asthma oder auch Allergien der Haut, wie Neurodermitis oder eine Kontaktallergie. Je nach der Gruppe der auslösenden Allergene spricht man von einer Hausstaubmilben-Allergie, Pollenallergie, Tierhaarallergie, Schimmelpilzallergie, Insektengiftallergie oder auch Nahrungsmittelallergie. Die allergischen Beschwerden können sich in Form von juckenden Hautausschlägen, juckenden tränenden Augen, Niesen, Husten und Atemnot oder auch Bauchschmerzen zeigen. Die Symptome können auch untypisch sein und sind oft unterschiedlich stark ausgeprägt. Die schwerste Form einer Allergie ist der allergische Schock, auch als Anaphylaxie bezeichnet. Übrigens: Auch Tiere können an einer Allergie erkranken.
Was ist ein Allergen?
Allergene können natürlichen oder nicht natürlichen Ursprungs sein. Natürlicherweise kommen Allergene zum Beispiel in Pollen oder anderen Pflanzenbestandteilen, Hausstaubmilben, Insektengift, Tierhaaren oder Nahrungsmitteln vor. Aber auch nicht natürliche Substanzen wie Konservierungsstoffe, Medikamente, Tattoofarben, Nickel etc., können Allergien auslösen; Nickel zum Beispiel kann ein allergisches Kontaktekzem auslösen.
Wie kommt es zu Allergien? Was sind die Ursachen?
Die Ursachen von Allergien sind nicht vollständig bekannt. Man kennt jedoch Faktoren, die eine Atopieneigung, das heißt, eine Neigung Allergien zu entwickeln, bei Kindern begünstigen. Zum einen sind dies erbliche Faktoren: Kinder von Eltern, die an einer Allergie leiden, haben ein höheres Risiko als andere, selbst auch Allergiker zu werden. Zum anderen spielen aber Umweltfaktoren eine glle: Eine seit Langem immer mehr erforschte Theorie dazu ist die sogenannte Hygiene-Hypothese. Diese Hypothese entstand, als sich in großen Studien zeigte, dass Kinder, die auf einem Bauernhof mit Tierställen aufwuchsen, deutlich seltener an Allergien erkrankten als Kinder, die in der Stadt lebten. Offenbar entsteht eine Art Schutz vor einer allergischen Überreaktion des Immunsystems, wenn sich das Immunsystem schon sehr früh mit verschiedenen Substanzen auseinandersetzen muss, die vor allem in der Nähe von Bauernhöfen beziehungsweise im Kuhstall vorkommen. Das Immunsystem ist nämlich mit der Geburt keinesfalls ausgebildet, sondern wird in den ersten Lebensjahren sozusagen trainiert – tauchen die „richtigen“ Substanzen auf, mit denen es trainiert wird, dann kann sich ein ausgewogen arbeitendes Immunsystem entwickeln. Es entsteht dann eine sogenannte Toleranz; eine Art „Gelassenheit“ gegenüber Substanzen, also ein Schutz vor allergischen Reaktionen.
Funktioniert dieses „Training“ − aus welchen Gründen auch immer − nicht so gut, kann sich eine Allergiebereitschaft und dann oft auch eine allergische Krankheit entwickeln. Weitere Umweltfaktoren können Allergien noch fördern; dazu gehört zum Beispiel auch die Luftverschmutzung. Auch die Klimaerwärmung kann negativ beitragen: Durch die zunehmende Erwärmung und damit längeren Vegetationsperioden verschiedener Pflanzen fliegen die Pollen häufig über längere Zeit im Jahr. Und in nördlichen Gebieten siedeln sich auch allergene Pflanzen an, die eigentlich nur in südlicheren Breiten zuhause waren, und führen dort zu neuen Allergien.
Wie häufig sind Allergien?
Allergien sind mittlerweile weltweit die häufigste chronische Erkrankung, wie Prof. Dr. med. Torsten Zuberbier, Direktor des Instituts für Allergieforschung an der Charité Berlin und Stiftungsvorsitzender ECARF, feststellt, Tendenz steigend.*
| Häufigkeit allergischer Erkrankungen in der EU | ||
| Allergie | Anzahl Betroffene | Bevölkerungsanteil in Prozent |
| Allergischer Schnupfen – Heuschnupfen | 134,5 Mio. | 30 % |
| Allergisches Asthma | 67,2 Mio. | 15 % |
| Handekzeme | 44,8 Mio. | 10 % |
| Lebensmittelallergien | 22,4 Mio. | 5 % |
| Quelle: Prof. Dr. med. Torsten Zuberbier, www.mein-allergie-portal.com | ||
Allerdings nimmt nicht nur die Anzahl der von Allergien Betroffenen zu, sondern auch der Schweregrad. So leiden mittlerweile sehr viele Pollenallergiker zusätzlich noch an einer Kreuzallergie auf Nahrungsmittel. Ein Teil des Problems ist auch, dass Allergien noch immer nicht ernst genug genommen werden, stellt Prof. Zuberbier fest – lediglich 10 Prozent der Allergiker werden korrekt behandelt. Das ist nicht nur für die Betroffenen eine ungünstige Entwicklung. Auch der volkswirtschaftliche Schaden, der durch unbehandelte Allergien entsteht, ist enorm, in der EU geht man von 100 Milliarden Euro aus, die durch eine adäquate Behandlung vermeidbar wären.
*Pressekonferenz Stiftung Deutscher Polleninformationsdienst (PID) und European Centre for Allergy Research Foundation (Stiftung ECARF), 14. Februar 2023, 10:30 Uhr bis 11:30 Uhr Kaiserin Friedrich-Haus, Hörsaal Robert-Koch-Platz 7 in 10115 Berlin
Auf was kann man allergisch sein?
 Übersicht: Auf was kann man allergisch sein? Bildquelle: MeinAllergiePortal
Übersicht: Auf was kann man allergisch sein? Bildquelle: MeinAllergiePortal
Allergische Reaktionen sind auf fast alles möglich. So kommt es zum Beispiel zu den folgenden Erkrankungen:
- Pollenallergien, zum Beispiel Baumpollen-Allergie, Gräser-Allergie, Beifuß-Allergie, Ambrosia-Allergie
- Hausstaubmilbenallergie
- Schimmelpilzallergie
- Allergie auf Tiere, wie Hunde, Katzen, Pferde
- Allergie auf Insektengift: Bienengiftallergie, Wespengiftallergie
- Allergie auf Medikamente bzw. deren Bestandteile: Penizillinallergie, Allergie auf PEG
- Allergie auf Nahrungsmittel, wie Kuhmilch, Hühnerei, Weizen, Erdnuss, Baumnüsse und zunehmend auch Cashew sowie zahlreiche weitere Lebensmittel.
Kann man Allergien vorbeugen?
Auch die Frage, ob es möglich ist, Allergien vorzubeugen, ist nicht geklärt. Sicher scheint zu sein, dass Kinder, die sich schon als Babys im Kuhstall aufhielten, deutlich seltener Allergien haben als Kinder, bei denen dies nicht so war. Das haben verschiedene „Bauernhof-Studien“ gezeigt. Allerdings leben nun einmal die meisten Kinder in städtischer Umgebung.
Als sicher gilt mittlerweile jedoch, dass man gesunde Kinder auf keinen Fall vor jeglichem Kontakt mit potenziellen Allergenen abschirmen sollte, wie dies lange Zeit empfohlen wurde. Wie man mittlerweile weiß, trägt es eher zum Schutz vor Allergien bei, wenn Säuglinge zwar gestillt werden, aber zusätzlich ab dem 4. Lebensmonat andere Nahrungsmittel erhalten. Dies sollten nicht, wie früher empfohlen, nur wenige Nahrungsmittel sein, die selten zu Allergien führen, sondern eher auch Hühnerei, Getreide, Fisch oder ähnliche Lebensmittel – im Grunde das, was die übrigen Familienmitglieder auch essen.
Besteht allerdings bei einem Kind ein hohes Allergierisiko, weil zum Beispiel die Eltern Allergiker sind, oder leidet der Säugling sogar bereits an einer allergischen Krankheit, dann ist bei der Ernährung eher Vorsicht geboten und es gelten besondere Empfehlungen. Dann lässt man sich am besten von einem Arzt beraten.
Wie sehen allergische Symptome aus?
Von der Allergie können unterschiedliche Organsysteme betroffen sein, sowohl isoliert als auch in Kombination. Es sind dies am häufigsten:
- Atemwege
- Haut
- Magen-Darm-Trakt
- Herz-Kreislauf-System
Symptome bei Allergien der Atemwege
Sind die Atemwege von einem allergischen Schnupfen (allergische Rhinitis/Heuschnupfen) betroffen, zum Beispiel bei Hausstaubmilbenallergie oder Tierhaarallergie, äußert sich dies in der Regel durch folgende Symptome an den oberen Atemwegen:
- juckende Nase
- verstopfte Nase oder meist eherverstärkte Nasensekretion
- Niesanfälle
- tränende, juckende, gerötete Augen
- möglicherweise auch Mattigkeit, Schlafstörungen, Leistungseinschränkungen
Leidet eine Person an einer allergischen Rhinitis, dann sind diese Symptome sind unabhängig vom Auslöser der Allergie. Es spielt also keine Rolle, ob eine Pollenallergie, eine Hausstaubmilbenallergie, eine Schimmelpilzallergie oder eine Tierhaarallergie die Ursache ist.
Ein allergisches Asthma bronchiale kann sich unter anderem mit den folgenden Symptomen an den unteren Atemwegen bemerkbar machen:
- Husten; trocken oder mit Auswurf
- pfeifende Atemgeräusche (Giemen)
- Kurzatmigkeit beziehungsweise Atemnot
- Beklemmungsgefühl in der Brust
Symptome bei Allergien der Haut
Auch an der Haut kann es zu allergischen Symptomen kommen. Diese sehen, je nach Erkrankung, ganz unterschiedlich aus.
Neurodermitis-Symptome
Bei einer Neurodermitis, auch atopische Dermatitis oder atopisches Ekzem genannt, liegt eine sogenannte Barrierestörung der Haut vor. Infolge einer genetischen Veranlagung sind die Hautzellschichten nicht so „dicht“ wie bei Gesunden. Die Haut verliert dadurch vermehrt Feuchtigkeit, wird trocken und rau. Dadurch können potenzielle Allergene, aber auch Keime aus der Umwelt leichter in die Haut eindringen. Meist besteht Juckreiz, der immer wieder sehr stark werden kann. Zusätzlich liegt bei Patienten mit atopischem Ekzem eine angeborene Störung verschiedener Immunzellen vor; dies ist die Ursache für die chronische allergische Reaktion der Haut bei den Betroffenen.
Bei Neurodermitis kommt es zu Ekzemen. Diese können sich durch Rötung, Schuppung, Nässen, Knötchen oder Bläschen bemerkbar machen. Je nach Alter der Patienten sind meist unterschiedliche Körperregionen betroffen: bei Säuglingen und Kleinkindern treten die Veränderungen meist an Kopf, Gesicht, Hals und Streckseiten der Extremitäten auf. Bei älteren Kindern, Jugendlichen und Erwachsenen sind oft Arm- und Kniebeugen, Hände, Gesicht und Hals oder Nacken betroffen. Aber: Neurodermitis kann prinzipiell überall auftreten. Zudem können die Symptome sehr unterschiedlich stark ausgeprägt sein und von kleinen, leicht schuppenden rötlichen Hautstellen bis zu großflächig extrem wunder, rissiger, nässender Haut reichen, die stark juckt.
Der Juckreiz, medizinisch Pruritus genannt, wird von den Patienten als besonders quälend empfunden. Der Juckreiz kann dazu führen, dass die Nachtruhe erheblich gestört und dadurch die Leistungsfähigkeit am Tag stark eingeschränkt sein kann. Ausgelöst durch das Kratzen, das in der Nacht meist nicht kontrollierbar ist, verstärkt sich die chronische Entzündung der Haut, es entstehen zudem Wunden, durch die Infektionserreger leichter und verstärkt in die Haut eindringen können. Das führt häufig zu einem Neurodermitisschub.
Als Sonderformen der Neurodermitis gelten die knotige Form und auch die sehr häufige münzförmige Form.
Allergisches Kontaktekzem: Symptome
Das Kontaktekzem kann sich durch eine Vielzahl von Symptomen äußern:
- Juckreiz
- Rötung der Haut
- Trockene, schuppende Haut
- Entzündete, verdickte Haut
- Knötchen oder Bläschen
- Schmerzhafte, schlecht heilende Risse
Symptome bei Allergien auf Nahrungsmittel
Allergische Reaktionen auf Nahrungsmittel sind sehr vielfältig und können jedes Organ betreffen, oft den Magen-Darm-Trakt. Man unterscheidet primäre Nahrungsmittelallergien, bei denen die allergische Reaktion durch das Allergen des jeweiligen Lebensmittels ausgelöst wird, und sekundäre Nahrungsmittelallergien. Bei den pollenassoziierten Nahrungsmittelallergien kommt es bei Pollenallergikern zu sogenannten Kreuzreaktionen auf bestimmte Nahrungsmittel, deren Allergene dem jeweiligen Pollenallergen ähneln. So reagieren zum Beispiel Birkenpollenallergiker häufig auch auf Apfel; grundsätzlich sind viele verschiedene Allergene bekannt, die sehr ähnlich in verschiedenen Pflanzen vorkommen und zu solchen Kreuzreaktionen führen können.
Symptome einer primären Allergie auf Nahrungsmittel
Auf so gut wie alle Nahrungsmittel kann man eine Allergie entwickeln. Häufig kommt es auf Kuhmilch, Weizen, Hühnerei und Erd- und Baumnüsse zu Allergien.
Folgende Symptome können bei einer Allergie auf Nahrungsmittel auftreten:
- Durchfall
- Bauchschmerzen
- Erbrechen
- Urtikaria (Nesselsucht)
- Laufende Nase
- Husten
- Blutdruckabfall
- Kreislaufzusammenbruch mit anaphylaktischem Schock
Symptome bei pollenassoziierten Nahrungsmittelallergien oder Kreuzallergien
Bei pollenassoziierten Nahrungsmittelallergien ist das sogenannte Orale Allergiesyndrom sehr häufig. Dann kann es nach Verzehr des entsprechenden Nahrungsmittels zu den folgenden Symptomen kommen:
- Schwellung der Lippen
- Schwellungen in der Mundhöhle
- Schwellung der Zunge
- Pelziges Gefühl auf der Zunge
- Juckreiz im Rachen
- Bläschen auf der Zunge oder an den Lippen
Insbesondere in der für die Patienten relevanten Pollensaison kann es zum Oralen Allergiesyndrom kommen.
Symptome bei Allergien auf Insektengift bzw. Allergie auf Bienengift oder Wespengift
Die Symptome bei einer Bienengiftallergie oder Wespengiftallergie können vielfältig sein. Möglich sind:
- Hautreaktionen (Schwellungen, Rötungen, Juckreiz)
- Atemwegsbeschwerden
- Magen-Darm-Beschwerden
- Herz-Kreislauf-Beschwerden
- Anaphylaktischer Schock
- Kommt es zu einem schweren anaphylaktischen Schock, kann es sogar zum Tod kommen.
Anaphylaxie: Allergische Symptome am Herz-Kreislauf-System
Wenn bei einer allergischen Reaktion das Herz-Kreislauf-System betroffen ist, besteht die Gefahr eines allergischen Schocks. Ein allergischer Schock, auch als anaphylaktischer Schock oder Anaphylaxie bezeichnet, ist die gravierendste Form einer Allergie.
Folgende Symptome können im Rahmen einer anaphylaktischen Reaktion auftreten:
- Haut: Flächenhafte Rötungen (Flush), Juckreiz, Kribbeln, Quaddeln (Urtikaria, Nesselsucht), Schwellungen vor allem im Gesicht (Angio- bzw. Quincke-Ödem)
- Augen: Bindehautrötung (Konjunktivitis)
- Magen-Darm-Trakt: Übelkeit, Bauchschmerzen, Erbrechen, Durchfall
- Atemwege: Schnupfen (Rhinitis), Heiserkeit, Kehlkopfschwellung, Atemnot, Husten, Atemstillstand
- Herz-Kreislauf-System: Pulsbeschleunigung (Tachykardie), im weiteren Verlauf bei Verschlechterung des Zustands aber auch Pulsverlangsamung (Bradykardie), Blutdruckabfall (Schwindel, Schwächegefühl, „Schwarzwerden vor Augen“, Schwitzen), Kreislaufschock, Kreislaufstillstand
Bei schwersten Reaktionen kann es zu Stuhl- und Harnabgang, zu Krämpfen und Bewusstlosigkeit kommen. Der Schweregrad der Anaphylaxie wird in Grad I−IV eingeteilt..
Allergien bei Kindern
Die Neigung, Allergien zu entwickeln, ist erblich. Sind die Eltern betroffen, haben die Kinder ein höheres Risiko als andere Kinder, an einer Allergie zu erkranken.
Was bedeutet „Etagenwechsel“ in Bezug auf Allergien?
Besteht bereits eine Allergie, kann es auch zu einem „Etagenwechsel“ kommen. Das bedeutet, dass sich zum Beispiel aus einer Pollenallergie mit Heuschnupfen nach einiger Zeit ein allergisches Asthma entwickeln kann.
Allergie-Diagnose: Welche Allergie-Tests gibt es?
Es gibt zur Diagnose von Allergien eine Vielzahl von Tests. Diese Tests dienen dazu, den Allergieverdacht, der sich im Rahmen der Anamnese ergeben hat, zu bestätigen oder auch zu widerlegen. Deshalb steht am Anfang jeder Allergie-Diagnose die sorgfältige Klärung der beobachteten Symptome. Um sich hier Klarheit zu verschaffen, sind oft Symptom-Tagebücher hilfreich, in denen man alle Beschwerden notiert und zum Beispiel festhält, wann man evtl. Pollen ausgesetzt war oder was man wann gegessen hat.
Folgende Allergietests kann der Arzt durchführen:
- Prick-Test (Auftragen verschiedener Allergene auf die Haut und Bewertung der Reaktion)
- Epikutantest (Hauttest)
- Nasaler Provokationstest (unter ärztlicher Überwachung)
- Oraler Provokationstest (unter ärztlicher Überwachung)
- IgE-Test (Bluttest)
- RAST (Bluttest)
- Molekularer Allergiediagnostik/Komponentendiagnostik (Bluttest)
Molekulare Allergiediagnostik – Komponentendiagnostik: Was bedeutet das?
Für klassische IgE-Allergietests werden Allergenextrakte verwendet. Diese Allergenextrakte werden aus einer Allergenquelle hergestellt, zum Beispiel aus Birkenpollen, und enthalten eine Mischung aus allergenen und nicht allergenen Komponenten. Die molokulare Allergiediagnostik oder Komponentendiagnostik arbeitet nicht mit Allergenextrakten, sondern mit sogenannten Allergenkomponenten, das sind einzelne allergene Proteine. So erlaubt die molekulare Allergiediagnostik eine sehr präzise Diagnose, denn sie identifiziert nicht nur die Allergenquelle, zum Beispiel Birke, sondern die relevante Allergenkomponenten, zum Beispiel Bet v 1. Dies führte Univ.-Prof. Dr. med. Thilo Jakob, Direktor der Klinik für Dermatologie und Allergologie am Universitätsklinikum Gießen (UKGM) bei der Fachkreise-Veranstaltung „Allergologie im Kloster 2023“ *aus.
Hilfreich ist die molekulare Allergiediagnostik insbesondere in diesen Fällen:
Aufdecken von Kreuzreaktivitäten
- Pollen-assoziierte Nahrungsmittelallergien, das sind Kreuzallergien, lassen sich von primären, „echten“ Nahrungsmittelallergien unterscheiden
- Klinisch weniger relevante Pollen-Pollen Kreuzreaktivitäten, zum Beispiel auf Profiline oder Polcalcine, lassen sich von genuinen Sensibilisierungen gegen Markerallergene der einzelnen Pollenarten unterscheiden.
Beurteilung der Erfolgsaussichten der Immuntherapie bzw. Hyposensibilisierung
- Das Sensibilisierungsmuster gibt Auskunft über die Erfolgsaussichten einer Immuntherapie
- Präzisere Indikationsstellung bei Insektengiftallergie. Unterscheiden lassen sich echte Doppelsensibilisierungen auf Biene und Wespe von einer Doppelsensitivität, die durch eine Kreuzreaktion der Bienengift- bzw. Wespengift-Allergene verursacht wurde.
Risikoabschätzung
Gefährliche und wenige gefährliche Sensibilisierungen lassen sich besser unterscheiden. So gibt es zum Beispiel bei Erdnuss, Haselnuss, Walnuss und Soja jeweils Allergene, die ein geringes Risiko bergen und solch, bei denen ein hohes Risiko für schwere Allergische Reaktionen bzw. eine Anaphylaxie besteht.
*Quelle: Dr. med. Thilo Jakob, „Molekulare Allergiediagnostik: Klinischer Nutzen für die Patientenversorgung“, Allergologie im Kloster 13.5.2023
Wie verlässlich ist die alternative Allergiediagnostik?
Die alternative Medizin wird von vielen geschätzt. Geht es jedoch um die Diagnose von Allergien, sind die hier genutzten Tests nicht empfehlenswert. Angeboten werden unter anderem:
- Bioresonanz
- Kinesiologie
- Dunkelfeldmikroskopie
- Zytotoxische Leukozytentests
- IgG4-Tests
- Keines dieser Verfahren ist dazu geeignet, den Nachweis einer Allergie zu erbringen.
Allergie-Therapie: Wie sieht die Behandlung aus?
Die grundsätzliche Therapie bei einer Allergie besteht darin, das Allergen möglichst zu vermeiden. Bei einer Berufsallergie kann es deshalb erforderlich sein, die Tätigkeit oder gar den Beruf zu wechseln. Handelt es sich jedoch z.B. um eine Pollenallergie, zum Beispiel Heuschnupfen, ist eine Allergenvermeidung nicht immer möglich. Man versucht deshalb in der Allergologie, wann immer dies möglich ist, durch eine geeignete Therapie die Beschwerden möglichst deutlich zu lindern. Je nachdem, um welches Allergen es sich handelt, wird versucht, die entzündliche Reaktion des Immunsystems durch Antihistaminika oder topische Steroide zu bekämpfen, damit die Symptome möglichst erst gar nicht auftreten. Zusätzlich stehen weitere, auch sehr gezielt wirkende Medikamente gegen eine Allergie zur Verfügung; dazu gehören auch die sogenannten Biologika.
Wie kann man Allergene meiden?
Es gibt viele Möglichkeiten für Allergiker, den Kontakt zu Allergenen zu meiden. Den Pollenallergikern zum Beispiel, kann ein Blick auf den aktuellen Pollenflug-Gefahrenindex des Deutschen Wetterdienstes dabei helfen, „ihren Pollen“ aus dem Weg zu gehen.
Allergene meiden mit dem ECARF-Siegel
Es gibt aber mittlerweile auch zahlreiche Produkte, bei deren Herstellung auf Allergenfreiheit geachtet wurde. Man erkennt sie zum Beispiel am ECARF-Qualitätssiegel, mit dem Produkte aller Art, vom Waschmittel über die Hautcreme bis zum Luftreiniger und Brot, als allergenfrei gekennzeichnet werden.
Allergene meiden mit der CheckWise App
Ein weiteres praktisches Tool für Allergiker ist die CheckWise App Die CheckWise App erkennt mögliche Allergene in Lebensmitteln, Zusatzstoffe (E-Nummern), Duft- und Inhaltsstoffe sowie Zucker.
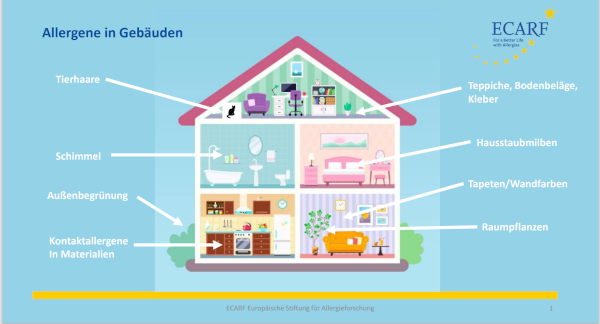
Allergenfreies Wohnen, geht das?
Der moderne Mensch hält sich überwiegend in Innenräumen auf. Gerade in Wohnungen, Häusern, Büros etc. gibt es aber viele Möglichkeiten mit potenziellen Allergenen in Kontakt zu kommen. Ob in Tapeten oder Bodenbelägen – überall lauern Allergene. Selbst die Außenbegrünung von Wohnanlagen ist häufig so gestaltet, dass Pollenallergiker negativ beeinträchtigt werden können.
Ein Lichtblick für Allergiker ist deshalb eine Initiative, die es sich zum Ziel gesetzt hat, Allergene in Gebäuden und in den Außenanlagen zu minimieren. Wie Angela Balatoni, Geschäftsführerin der Allergy Friendly Buildings Alliance GmbH (AFBA) erklärt* ist es relativ kostenneutral möglich, allergikerfreundlich zu bauen. Die AFBA bietet deshalb Expertise und Beratung für Bauherren, Planer, Architekten und Ingenieure.
 Angela Balatoni, Geschäftsführerin der Allergy Friendly Buildings Alliance GmbH (AFBA): "Es relativ kostenneutral möglich, allergikerfreundlich zu bauen!"
Angela Balatoni, Geschäftsführerin der Allergy Friendly Buildings Alliance GmbH (AFBA): "Es relativ kostenneutral möglich, allergikerfreundlich zu bauen!"
*Pressekonferenz Stiftung Deutscher Polleninformationsdienst (PID) und European Centre for Allergy Research Foundation (Stiftung ECARF), 14. Februar 2023, 10:30 Uhr bis 11:30 Uhr Kaiserin Friedrich-Haus, Hörsaal Robert-Koch-Platz 7 in 10115 Berlin
Allergie-Therapie: Allergspezifische Immuntherapie (AIT) oder Hyposensibilisierung
Eine zunehmend angewandte und auch erfolgreiche Therapie ist die AIT – die Allergenspezifische Immuntherapie oder auch Spezifische Immuntherapie (SIT) oder Hyposensibilisierung genannt. Dabei handelt es sich um eine Therapie mit dem Ziel, das Immunsystem gegen das Allergen "tolerant" zu machen. Eine AIT erfolgt in der Regel subkutan, d.h. unter die Haut gespritzt (SCIT) oder sublingual, d.h. als Tablette, die unter die Zunge gelegt und resorbiert wird (SLIT). Durch eine schrittweise Zufuhr des allergieauslösenden Allergens über meist 3 bis 5 Jahre soll eine Toleranz des Immunsystems gegenüber dem Allergen erreicht werden. Kommt es dann "auf natürlichem Wege" zu einem Allergenkontakt, ist das Immunsystem "gewappnet" und ordnet das Allergen nicht mehr als feindlich ein. Damit setzt die AIT nicht erst bei den Symptomen der Allergie an, sondern bei den Ursachen. Eine AIT kann in einigen Fällen damit auch den gefürchteten Etagenwechsel zum allergischen Asthma verhindern. Wenn die entsprechenden Voraussetzungen für die Durchführung einer AIT bestehen, kann diese deshalb so früh wie möglich zu Beginn des Krankheitsverlaufs erfolgen.
Experten stellen immer wieder fest, dass nicht alle Patienten, die davon profitiern würden, eine Hyposensibilisierung erhalten. Zu den Gründen dafür gibt es viele Vermutungen. Eine von MeinAllergiePortal durchgeführte nicht repräsentative Umfrage unter den Lesern zur Hyposensibilisierung brachte überraschende Ergebnisse.
Aktuell kann eine AIT u.a. bei Allergien gegen die folgenden Allergene eingesetzt werden:
- Bienengift/Wespengift
- Pollen, z.B. Baumpollen, Gräserpollen und Kräuterpollen
- Hausstaubmilben
- Schimmelpilze
- Tierhaare
Zur Therapie der Erdnuss-Allergie ist seit neustem eine orale Therapie zugelassen.
Allergie-Therapie mit Biologika
Neue Therapieoptionen bieten auch die neuen Biologika. Mit "Biologika" oder auch Biopharmazeutika bezeichnet man Medikamente, die mit Hilfe von gentechnisch veränderten Organismen, d.h. "biotechnologisch", hergestellt werden. Bei der Behandlung von Allergien ist der Einsatz von Biologika beschränkt auf Patienten, deren Allergiesymptome trotz der anderen Therapiemöglichkeiten sehr schwer ausgeprägt sind. Die Wirkstoffe sind sogenannte monoklonale Antikörper, die selektiv bestimmte Botenstoffe im Immunsystem blockieren, die an der Überreaktion des Immunsystems beteiligt sind – damit dämpfen sie die allergische Reaktion.
Allergie-Therapie mit JAK-Inhibitoren
„JAK-Inhibitoren“, kurz für Januskinase-Inhibitoren, werden aktuell unter anderem zur Behandlung von schweren Formen der Neurodermitis entwickelt; ein erster Wirkstoff ist bereits zugelassen. Sie hemmen ebenfalls gezielt Entzündungsprozesse, sodass die Entzündungsreaktion abgeschwächt oder sogar unterbunden werden kann. JAK-Inhibitoren eignen sich deshalb zur Therapie von bestimmten Erkrankungen, die mit chronischen Entzündungsprozessen einhergehen.
Welcher Arzt hilft bei Allergien?
Generell ist die erste Anlaufstelle bei Allergieverdacht der Hausarzt. Auch Fachärzte wie der Hals-Nasen-Ohren-Arzt oder der Dermatologe können helfen. Ärzte mit der Zusatzbezeichnung „Allergologie“ haben sich auf die Diagnose und Behandlung von Allergien spezialisiert. Darüber hinaus gibt es allergologische Zentren an einigen Kliniken.
Wichtiger Hinweis
Unsere Beiträge beinhalten lediglich allgemeine Informationen und Hinweise. Sie dienen nicht der Selbstdiagnose, Selbstbehandlung oder Selbstmedikation und ersetzen nicht den Arztbesuch. Die Beantwortung individueller Fragen durch unsere Experten ist leider nicht möglich.
Autor: Dr. med. Susanne Meinrenken, Prof. Dr. med. Torsten Zuberbier, Angela Balatoni, Prof. Dr. med. Thilo Jakob, www.mein-allergie-portal.com
Lesen Sie auch
-
Allergien, Unverträglichkeiten, oder ist es die Psyche?
-
Allergie und Impfen: Ein Risiko für allergische Reaktionen?
-
Alternative Behandlung bei Allergien
Weitere Beiträge
News - Allergie Allgemein
- Update Allergologie - Immunologie: Was ist neu?
- 20 Jahre Allergologie im Kloster: Neues zu Diagnostik & Therapie
- Deutscher Allergiekongress 2023: Ein Blick in die Zukunft
- CFS: Wie kommt es zum chronischen Fatigue-Syndrom?
- Alternative Heilmethoden bei Allergien, geht das?
- Allergie – was ist das?
- Allergien dank molekularer Allergologie verhindern?
- Biologika bei Asthma, Neurodermitis, Urtikaria, Nasenpolypen
MeinAllergiePortal wird unterstützt von